O que é Alzheimer e onde o Aducanumab se encaixa?
A Doença de Alzheimer representa o tipo mais comum de demência, afetando milhões de pessoas globalmente. Caracteriza-se pela progressiva deterioração das funções cognitivas, como memória, raciocínio e capacidade de realizar tarefas cotidianas. Historicamente, as opções terapêuticas limitavam-se a medicamentos que apenas aliviavam sintomas temporariamente, sem modificar a progressão da doença. Neste cenário, o Aducanumab emerge como uma abordagem inovadora, sendo o primeiro medicamento aprovado nos Estados Unidos (em 2021) com o potencial de alterar o curso biológico da enfermidade ao atacar uma de suas causas fundamentais.
Como o Aducanumab Funciona?
O medicamento é um anticorpo monoclonal desenvolvido para reconhecer e eliminar depósitos anormais de proteína beta-amilóide no cérebro. Segundo a hipótese amilóide predominante na pesquisa do Alzheimer, o acúmulo dessa proteína forma placas que danificam neurônios e sinapses, desencadeando a cascata de eventos que levam à demência. O Aducanumab liga-se especificamente às formas agregadas da beta-amilóide, promovendo sua remoção pelos mecanismos de defesa naturais do cérebro.
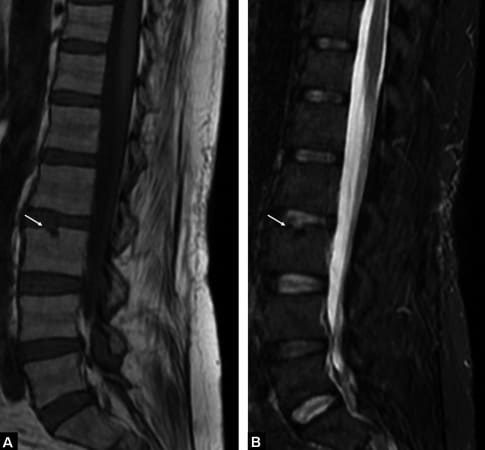
Este processo exige administração contínua via infusão intravenosa a cada quatro semanas. Estudos de imagem mostram redução significativa das placas amiloides após 6-12 meses de tratamento, embora a tradução clínica em melhora cognitiva permaneça um ponto de discussão científica.
Abordagens Terapêuticas Não Cirúrgicas para Alzheimer
Antes do advento do Aducanumab, o arsenal terapêutico focava no manejo sintomático. Atualmente, a estratégia ideal combina múltiplas abordagens:
| Estágio da Doença | Medicações | Intervenções Não-Farmacológicas |
|---|---|---|
| Inicial | Inibidores da colinesterase (Donepezil, Rivastigmina) | Estimulação cognitiva, exercícios físicos regulares, dieta Mediterrânea |
| Intermediário | Memantina + Inibidores da colinesterase | Terapia ocupacional, grupos de apoio para cuidadores, adaptação ambiental |
| Avançado | Memantina isolada, manejo de sintomas comportamentais | Cuidados paliativos, prevenção de complicações (como infecções) |
O Aducanumab destina-se especificamente para estágios iniciais da doença, onde a patologia amiloide está ativa mas o dano neuronal ainda é parcialmente reversível. Sua inclusão no protocolo terapêutico representa uma mudança de paradigma: da abordagem puramente sintomática para estratégias que atacam a fisiopatologia subjacente.
Quem Pode se Beneficiar com o Aducanumab?
A indicação é rigorosamente específica. Candidatos ideais apresentam:
- Diagnóstico confirmado de Alzheimer em estágio leve ou comprometimento cognitivo leve (MCI) devido a Alzheimer
- Presença comprovada de depósitos de beta-amilóide no cérebro via PET scan ou análise do líquido cefalorraquidiano
- Idade geralmente entre 50-85 anos
- Ausência de micro-hemorragias cerebrais significativas pré-existentes
Riscos e Monitoramento Essencial
O principal efeito adverso do Aducanumab é a ARIA (Abnormalidades de Imageamento Relacionadas à Amiloide), que inclui edema cerebral (ARIA-E) e micro-hemorragias (ARIA-H). Estes eventos ocorrem em até 35% dos pacientes, sendo mais frequentes em portadores do gene APOE ε4. Embora muitos casos sejam assintomáticos, alguns podem apresentar:
| Sintoma | Ação Recomendada |
|---|---|
| Dor de cabeça intensa e persistente | Procurar serviço de emergência imediatamente |
| Confusão súbita ou sonolência excessiva | Contatar equipe médica no mesmo dia |
| Tontura com perda de equilíbrio | Suspender atividades e consultar médico em 24h |
| Visão dupla ou tremores novos | Agendar avaliação neurológica urgente |
O protocolo de segurança exige ressonâncias magnéticas antes do início do tratamento, aos 5-7 meses e aos 12 meses. Pacientes com ARIA sintomática necessitam interrupção temporária ou definitiva da terapia.
Perspectivas Futuras e Pesquisas em Andamento
O Aducanumab inaugurou uma nova era terapêutica, porém não é o fim da jornada. Atualmente, mais de 120 ensaios clínicos investigam novas estratégias:
Abordagens promissoras incluem anticorpos contra a proteína tau (responsável por emaranhados neurofibrilares), moduladores da inflamação cerebral, e terapias genéticas. No Brasil, centros de referência como o Hospital das Clínicas de São Paulo e o Instituto do Cérebro do Rio Grande do Sul participam ativamente destes estudos, oferecendo acesso a protocolos experimentais para pacientes elegíveis.
Orientações Práticas para Pacientes e Familiares
Nunca interrompa medicamentos atuais sem orientação. O Aducanumab não substitui terapias sintomáticas como Donepezil ou Memantina. A abordagem ideal mantém todos os tratamentos estabelecidos enquanto avalia os benefícios desta nova opção.
Invista em um diário clínico digital para registrar alterações sutis de humor, sono e capacidade funcional. Estes dados são valiosos para o médico avaliar a resposta terapêutica em consultas de acompanhamento.
Participe de grupos de apoio credenciados pela ABRAZ (Associação Brasileira de Alzheimer). O suporte emocional e troca de experiências práticas são fundamentais para a adaptação à nova rotina de tratamento.
Perguntas Frequentes sobre Aducanumab
O Aducanumab está disponível no SUS ou planos de saúde?
Atualmente, o medicamento não está registrado na ANVISA e não é oferecido pelo SUS. Alguns planos de saúde cobrem o tratamento mediante aprovação judicial, mas o custo anual excede R$ 350.000,00. A ANVISA analisa o pedido de registro desde 2022, sem previsão de conclusão.
Quanto tempo leva para ver resultados?
As reduções nas placas amiloides são visíveis em exames de imagem após 6 meses, mas benefícios cognitivos significativos podem levar 12-18 meses para se manifestar. Cerca de 30% dos pacientes apresentam estabilização cognitiva em comparação com a progressão esperada.
Posso tomar outros remédios para Alzheimer junto?
Sim, o Aducanumab é compatível com inibidores de colinesterase (Donepezil, Rivastigmina) e Memantina. Na verdade, a combinação é recomendada pois atua em mecanismos complementares. Sempre informe seu médico sobre todos os medicamentos em uso.
Existem alternativas mais acessíveis?
Outros anticorpos anti-amilóide como Lecanemab e Donanemab mostraram resultados mais consistentes em estudos recentes e estão em fase avançada de avaliação regulatória. Espera-se que sua chegada ao mercado aumente a competição e reduza custos a longo prazo.
Como é a aplicação do medicamento?
Administrado por infusão intravenosa em ambiente hospitalar ou clínica especializada. Cada sessão dura aproximadamente 1 hora, realizada a cada 4 semanas. Pacientes devem permanecer em observação por 1-2 horas após a infusão para monitorar reações imediatas.
Quais exames são obrigatórios antes de iniciar?
Ressonância Magnética cerebral prévia, teste confirmatório de beta-amilóide (PET ou análise de líquor), eletrocardiograma e avaliação completa de função renal e hepática. Teste genético para APOE ε4 é opcional mas recomendado para estratificação de risco.
O tratamento precisa ser vitalício?
Atualmente não há dados conclusivos sobre duração ideal. Estudos sugerem que a interrupção pode levar ao reaparecimento de placas amiloides em 6-12 meses. A recomendação é manter o tratamento indefinidamente enquanto houver benefício clínico e ausência de efeitos adversos graves.
Idosos acima de 85 anos podem usar?
A segurança nesta faixa etária não foi estabelecida nos ensaios clínicos originais. A decisão deve ser individualizada, considerando fragilidade do paciente, comorbidades e expectativa de vida. Risco de ARIA é significativamente maior neste grupo.
Como a dieta influencia o tratamento?
Padrões alimentares como a dieta MIND (combinação de Mediterrânea e DASH) demonstraram reduzir progressão cognitiva em 53% em estudos observacionais. Alimentos ricos em antioxidantes (mirtilo, espinafre) e ômega-3 (peixes) potencializam os efeitos neuroprotetores do tratamento.
Existe risco de dependência?
Não. O Aducanumab não é psicoativo e não causa dependência física ou psicológica. Trata-se de um anticorpo que age especificamente no sistema nervoso central sem afetar receptores cerebrais associados a vícios.
Posso continuar dirigindo?
A capacidade de dirigir deve ser reavaliada trimestralmente por um neurologista. Efeitos colaterais como tontura, sonolência ou alterações visuais podem comprometer temporariamente essa habilidade. Priorize segurança: utilize transporte alternativo até liberação médica.
O plano de saúde pode negar cobertura?
Sim, pois o medicamento não possui registro na ANVISA. A cobertura depende de ação judicial comprovando a necessidade do tratamento e a ausência de alternativas terapêuticas equivalentes. A成功率 de liminares favoráveis é de aproximadamente 65% segundo dados da ANS.
Como lidar com os custos elevados?
Programas de acesso expandido (como o do próprio laboratório) oferecem descontos progressivos baseados na renda familiar. Associe-se à ABRAZ para orientação jurídica gratuita sobre processos de cobertura e busque centros universitários que participam de estudos clínicos com medicamentos gratuitos.
O tratamento ajuda em demências não-Alzheimer?
Não. O Aducanumab é específico para a patologia amiloide característica do Alzheimer. Em demências vasculares, por corpos de Lewy ou frontotemporais, o medicamento não demonstra benefício e pode aumentar riscos desnecessariamente. Diagnóstico preciso é essencial.
Quais exercícios são recomendados durante o tratamento?
Atividades aeróbicas moderadas (30 minutos diários de caminhada) associadas a exercícios de equilíbrio (como tai chi) e estimulação cognitiva (quebra-cabeças, aprendizado de idiomas) demonstraram efeito sinérgico com terapias anti-amilóide. Evite exercícios de alto impacto durante as primeiras 24h após infusão.